2020年上海金山区高考考试化学一模试题
2020年上海金山区高考考试化学一模试题
1、选择题(共40分,每小题2分.每小题只有一个正确答案)
1. 关于![]() 中数字的描述正确的是( )
中数字的描述正确的是( )
A.![]() 是
是![]() 的质子数
的质子数
B.![]() 是
是![]() 的中子数
的中子数
C.![]() 是
是![]() 元素的相对原子水平
元素的相对原子水平
D.![]() 是
是![]() 元素的水平数
元素的水平数
2. 下列物质是混合物的是( )
A.冰醋酸 B.汽油 C.硫磺 D.丙三醇
3. 常温下,![]() 、
、![]() 在浓硫酸中钝化,浓硫酸表现了( )
在浓硫酸中钝化,浓硫酸表现了( )
A.难挥发性 B.吸水性 C.脱水性 D.强氧化性
4. 根据有机物的命名规则,下列命名正确的是( )
A.![]() ,
,![]() 二甲基戊烷 B.
二甲基戊烷 B.![]() ,
,![]() 二甲基戊烷
二甲基戊烷
C.![]() ,
,![]() 二甲基丁烷 D.
二甲基丁烷 D.![]() ,
,![]() ,
,![]() 三甲基丁烷
三甲基丁烷
5. 下列过程是物理变化的是( )
A.煤的干馏 B.石油的分馏 C.石油裂化 D.石油裂解
6. 关于乙醛,下列化学用语正确的是( )
A.官能团![]() B.比率模型
B.比率模型 
C.最简式 ![]() D.结构式
D.结构式 ![]()
7. 现有![]() 为
为![]() 的
的![]() 的
的![]() ,下列有关判断正确的是( )
,下列有关判断正确的是( )
A.溶液显酸性,主要由于铝离子水解致使的
B.溶液显酸性,主要由于溶液中有盐酸
C.溶液显碱性,主要由于铝离子水解致使的
D.溶液显碱性,主要由于铝离子水解致使的
8. 不可以辨别![]() 盐酸和
盐酸和![]() 溶液的是( )
溶液的是( )
A.石蕊试液 B.甲基橙试液 C.酚酞试液 D.淀粉![]() 试液
试液
9. 工业生产氨气的适合条件中不包含( )
A.用浓硫酸吸收产物 B.用铁触媒作催化剂
C.温度![]() 左右 D.压强为
左右 D.压强为![]()
10. 氮气常用作白炽灯泡中钨丝的保护气,这是由于( )
A.氮气比空气轻 B.氮气难溶于水
C.氮气是无色无味的气体 D.氮气非常不活泼
11. 下列物质对水的电离平衡没影响的是( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
12. ![]() 与
与![]() 分子都是正四面体结构。下列判断正确的是( )
分子都是正四面体结构。下列判断正确的是( )
A.键长:![]()
B.键能:![]()
C.沸点:![]()
D.共用电子对偏移程度:![]()
13. 准确量取![]() 溶液,比较合适的仪器是( )
溶液,比较合适的仪器是( )
A.![]() 量筒 B.
量筒 B.![]() 滴定管
滴定管
C.![]() 量筒 D.有刻度的
量筒 D.有刻度的![]() 烧杯
烧杯
14. 如图表示某可逆反应在用和未用催化剂时,反应过程和能量的对应关系。下列说法肯定正确的是( )
A.该反应为吸热反应
B.![]() 与
与![]() 相比,
相比,![]() 的反应速率更快
的反应速率更快
C.![]() 与
与![]() 相比,反应的平衡常数肯定不同
相比,反应的平衡常数肯定不同
D.![]() 大于
大于![]() ,说明总能量生成物比反应物低
,说明总能量生成物比反应物低
15. 下列转化过程不可能通过一步反应达成的是( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
16. 糕点包装中容易见到的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列剖析正确的是( )
A.脱氧过程中铁作为原电池正极
B.负极的电极反应为:![]()
C.正极的电极反应为:![]()
D.脱氧过程是吸热反应,可减少温度,延长糕点保质期
17. 一般情况下,仅凭下列事实能证明乙酸是弱酸的是( )
A.某乙酸溶液与锌粒反应产生气泡非常慢
B.乙酸钠溶液![]()
C.乙酸溶液能使石蕊变红
D.某乙酸溶液导电能力弱
18. 除去物质中含少量杂质的办法错误是( )
选项 | 物质(括号内为杂质) | 实验办法 |
|
| 加入稀硫酸使溶液呈中性 |
|
| 样品配制成热饱和溶液,冷却结晶,过滤 |
|
| 通过 |
| 溴苯(溴) | 加入足量 |
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
19. 下列关于晶体的叙述中,正确的是( )
A.原子晶体中,共价键的键能越大,熔、沸点越高
B.分子晶体中,分子间有哪些用途力越大,该分子越稳定
C.分子晶体中,共价键的键能越大,熔、沸点越高
D.某晶体溶于水后,可电离源于由移动的离子,该晶体肯定是离子晶体
20. 测得某![]() =
=![]() 的溶液中有关数据如表:则该溶液中还可能很多存在的一种离子是( )
的溶液中有关数据如表:则该溶液中还可能很多存在的一种离子是( )
离子 |
|
| ? |
|
|
浓度 |
|
| ? |
|
|
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
2、综合题,完成下列填空(共60分)
从宏观和微观两个角度认识氯、硫、铁、铝等元素的单质及其化合物是学好中学化学的要紧基础。
完成下列填空:
(1)![]() 在元素周期表中的地方为________,由此可知,其最高价氧化物对应的水化物的化学式为:________,次氯酸分子的结构式为:________。
在元素周期表中的地方为________,由此可知,其最高价氧化物对应的水化物的化学式为:________,次氯酸分子的结构式为:________。
(2)![]() 、
、![]() 、
、![]() 三种元素形成简单离子其半径由大到小的顺序是________(用离子符号表示)。铝最高价氧化物对应的水化物表现出了独特的性质,其在水溶液中的电离方程式为________。
三种元素形成简单离子其半径由大到小的顺序是________(用离子符号表示)。铝最高价氧化物对应的水化物表现出了独特的性质,其在水溶液中的电离方程式为________。
(3)硫和氯的非金属性强弱关系是________,试从原子结构的角度讲解其缘由。________。
(4)现有试剂:溴水、硫化钠溶液、![]() 溶液、稀硫酸、
溶液、稀硫酸、![]() 溶液、氨水。 要证明
溶液、氨水。 要证明![]() 具备还原性,应使用的试剂有________,看到的现象是________。要证明
具备还原性,应使用的试剂有________,看到的现象是________。要证明![]() 具备氧化性,应使用的试剂有
具备氧化性,应使用的试剂有
________,反应的离子方程式是________。
中国科学家用金属钠和![]() 在肯定条件下制得了金刚石:
在肯定条件下制得了金刚石:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() (金刚石)。
(金刚石)。
(1)配平上述反应的化学方程式:
若反应过程中有![]() 反应,则电子转移的数目为:________。
反应,则电子转移的数目为:________。
(2)![]() 的电子式为:________,
的电子式为:________,![]() 原子核外电子有________个能级。
原子核外电子有________个能级。
(3)已知:
常压下 | 钠 |
| 金刚石 | 石墨 |
熔点 |
|
|
|
|
沸点 |
|
| ---- |
|
若反应在常压、![]() 下进行,写出该反应的平衡常数表达式________。若
下进行,写出该反应的平衡常数表达式________。若![]() =
=![]() ,则________(选填序号)。
,则________(选填序号)。![]() .反应一定达到平衡
.反应一定达到平衡 ![]() .反应可能达到平衡
.反应可能达到平衡 ![]() .反应一定未达平衡
.反应一定未达平衡
(4)副产物![]() 溶于水后溶液呈碱性,请结合平衡移动的原理,用文字描述所得溶液呈碱性是什么原因:
溶于水后溶液呈碱性,请结合平衡移动的原理,用文字描述所得溶液呈碱性是什么原因:
________。若在![]() 升容器中,反应进行了
升容器中,反应进行了![]() ,金刚石的水平增加了
,金刚石的水平增加了![]() ,则
,则![]() 里
里![]() 的平均反应速率为________。
的平均反应速率为________。
爱国实业家侯德榜在氨碱法的基础上,创造了“联合制碱法”,简单步骤如图。完成下列问题: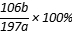
(1)写出通入![]() 和
和![]() 的化学反应方程式________。在饱和食盐水中通入
的化学反应方程式________。在饱和食盐水中通入![]() 和
和![]() ,先通
,先通![]() 后通
后通![]() 是什么原因________。
是什么原因________。
(2)母液中除![]() 和
和![]() 外,还含有些离子是________。 向母液中通氨气,加入细小食盐颗粒,冷却析出副商品,通氨气有哪些用途有________。
外,还含有些离子是________。 向母液中通氨气,加入细小食盐颗粒,冷却析出副商品,通氨气有哪些用途有________。![]() 增大
增大![]() 的浓度,使
的浓度,使![]() 更多地析出
更多地析出![]() 使
使![]() 更多地析出
更多地析出![]() 使
使![]() 转化为
转化为![]() ,提升析出的
,提升析出的![]() 纯度
纯度
(3)上述步骤中![]() 物质的分子式________。使材料氯化钠的借助率从
物质的分子式________。使材料氯化钠的借助率从![]() 提升到
提升到![]() 以上,主如果设计了________(填上述步骤中的编号)的循环。从沉淀池中取出沉淀的操作是________。
以上,主如果设计了________(填上述步骤中的编号)的循环。从沉淀池中取出沉淀的操作是________。
(4)写出检验商品碳酸钠中是不是含有氯化钠的简要策略:________。
(5)工业生产的纯碱常会含少量![]() 杂质。现用重量法测定其纯度,步骤如下:
杂质。现用重量法测定其纯度,步骤如下:
称取样品![]() ,加水溶解,加入足量的
,加水溶解,加入足量的![]() 溶液,经过滤、洗涤、干燥,最后得到固体
溶液,经过滤、洗涤、干燥,最后得到固体![]() 。样品中纯碱的水平分数为________(用含
。样品中纯碱的水平分数为________(用含![]() 、
、![]() 的代数式表示)。
的代数式表示)。
以甲醇和石油裂解气为材料可制得![]() ,已知
,已知![]() 由两种均具备芳香气味的有机物组成的混合物。有关物质转化关系如图:
由两种均具备芳香气味的有机物组成的混合物。有关物质转化关系如图:
请回答:
(1)写出![]() 中官能团的化学式________。
中官能团的化学式________。![]() 的结构简式是________。
的结构简式是________。
(2)![]() 的化学方程式是________、________。
的化学方程式是________、________。
(3)含有相同官能团的有机物一般具备一样的化学性质,因此可以预测![]() 具备与________ 类化合物一样的化学性质。除去化合物
具备与________ 类化合物一样的化学性质。除去化合物![]() 、
、![]() 和
和![]() 混合物中的
混合物中的![]() 、
、![]() ,可使用的办法是:________。
,可使用的办法是:________。
(4)写出一种以![]() 为材料制备
为材料制备 ![]() 的合成路线。
的合成路线。
参考答案与考试试题分析
2020年上海金山区高考考试化学一模试题
1、选择题(共40分,每小题2分.每小题只有一个正确答案)
1.
【答案】
A
2.
【答案】
B
3.
【答案】
D
4.
【答案】
C
5.
【答案】
B
6.
【答案】
C
7.
【答案】
A,B
8.
【答案】
D
9.
【答案】
A
10.
【答案】
D
11.
【答案】
A
12.
【答案】
B
13.
【答案】
B
14.
【答案】
D
15.
【答案】
B
16.
【答案】
C
17.
【答案】
B
18.
【答案】
B
19.
【答案】
A
20.
【答案】
A
2、综合题,完成下列填空(共60分)
【答案】
第三周期第![]() 族,
族,![]() ,
,![]()
![]() ,
,![]()
![]() ,氯和硫原子电子层数相同,质子数氯大于硫,因此氯原子核对最外层电子的吸引能力大于硫,得电子能力大于硫
,氯和硫原子电子层数相同,质子数氯大于硫,因此氯原子核对最外层电子的吸引能力大于硫,得电子能力大于硫
溴水,橙红色褪去,硫化钠溶液和稀硫酸,![]() =
=![]()
【答案】
![]()
![]() ,
,![]()
![]() ,
,![]()
因为碳酸是弱电解质,![]() 溶于水后电离出的碳酸根离子结合了水电离出的氢离子,致使水的电离平衡朝正反应方向移动,氢氧根离子浓度大于氢离子浓度,
溶于水后电离出的碳酸根离子结合了水电离出的氢离子,致使水的电离平衡朝正反应方向移动,氢氧根离子浓度大于氢离子浓度,![]()
【答案】
![]() =
=![]() ,氨气在水中溶解度大,先通氨气有益于生成碳酸氢钠沉淀
,氨气在水中溶解度大,先通氨气有益于生成碳酸氢钠沉淀
![]() 、
、![]() 、
、![]() 、
、![]() ,
,![]() 、
、![]()
![]() ,
,![]() ,过滤
,过滤
可取少量试样溶于水后,再滴加足量的稀硝酸和少量的硝酸银溶液,若产生白色沉淀不溶解,说明有![]()
![]()
【答案】
![]() ,
,![]()
![]() =
=![]() ,
,![]() =
=![]()
醛和酯,用饱和碳酸钠溶液洗涤后,通过分液操作除去